Tämä kirjoitus on jatkoa edelliselle osalle ”Piilevät hermoärsytykset ja neuroinflammaatio tyypillisissä TULE-vaivoissa”.
Osa kokonaisuutta
Yhä enemmän tiede alkaa ymmärtämään kuinka kehon eri biosysteemit vaikuttavat yhdessä hermoston tapaan tuottaa ja ylläpitää kipua. Yksi merkittävä toimintapari kivussa on autonominen hermosto ja autoimmuunisysteemi. Olet ehkä ajatellut samalla tavalla kuin minä aikaisemmin, että immuunipuolustuksen tehtävähän on tunnistaa, estää ja tuhota meille vaarallisia bakteereita, viruksia, jotka pyrkivät kehomme asukeiksi tai syöpäsoluja, jotka pyrkivät kehittymään ja jakautumaan kehossamme. On luontaista ja opittua immuunipuolustusta. Hieman liian herkäksi oppinut puolustus johtaa esimerkiksi allergioihin. On olemassa myös autoimmuunisairauksia, kuten reumaa, Chronin tautia, diabetesta, MS-tautia, CFS-syndromaa jne. Näissä sairauksissa kehon puolustusmekanismit alkavat hyökkäämään omia solujaan vastaan, joka aiheuttaa kroonisen tulehduksen, tämä on tuttua.
Nykyaikainen käsitys immunologiasta on sen vaikutus kivun kehittymiseen ja kroonistumiseen. Tämä aihe on ollut kipututkijoiden mielenkiinnon aiheena jo useamman vuoden, ja nyt tutkijoilla alkaa olla näyttöä, kuinka immunologiset puolustusreaktiot herkistävät hermostoa ja aiheuttavat kivun (Ren & Dubner, 2010; Totsch & Sorge, 2017). Mielenkiintoista on myös se, kuinka opittu immuunipuolustus voi oppia reagoimaan kipuun herkemmin aikuisiässä, jos hermosto on altistunut varhaisessa lapsuusvaiheessa merkittävän paljon kivulle (Giboney, 2004; Salter, 2018). Kivun herkkyys voi periaatteessa siis kehittyä kuin allergia.
Stressi lisää immuunipuolustusherkkyyttä
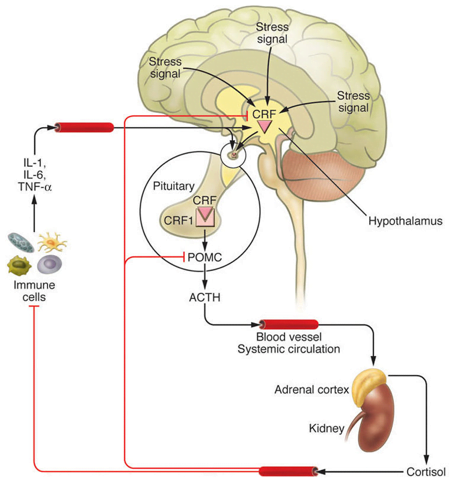
Kun stressireaktio kestää normaalia kauemmin, päiviä tai kuukausia, sen vaikutus muuttuu haitalliseksi. Aivomme kuvittelevat jonkin vaaran uhkaavan, ja ”pakene tai taistele” -hermostomme (sympaattinen hermosto) ottaa vallan. Se vähentää tietoisuudesta, päätöksenteosta ja suunnitelmallisuudesta vastaavan prefrontaalisen aivokuoren toimintaa ja puolestaan vahvistaa primitiivisten aivoalueiden aktiviteettia. Yksi näistä primitiivisistä aivo-osista on hypotalamus. Se säätelee hormonijärjestelmiä, jonka avulla se kontrolloi muun muassa kehon lämpötilaa, nälkää, kiihtymistä, janoa, väsymystä, unta ja sisäistä kelloa. (Abdallah C. 2017)
Pitkittyneessä stressitilassa hypotalamus lähettää munuaisen kuorikerrokselle käskyn alkaa lisäämään kortisolia, tätä hyvin tunnettua stressihormonia verenkiertoomme. Liiallinen kortisolin määrä veressä kiihdyttää immuunisolujen aktiviteettia, jotka alkavat tuottamaan enemmän inflammatorisia vasta-aineita – sytokiineja. Tätä ketjua kutsutaan hypotalamus-hypofyysi-akseliksi. Stressi siis lisää kehon tulehdusvastetta. (Sapolsky, 1998)
Unen puute voimistaa neuroinflammaatiota
Pitkittyneestä stressistä kulkee suora silta uniongelmiin. Edellä mainittu sympaattisen hermoston aktiviteetti ja liika kortisolin määrä veressä häiritsevät ihmisen fysiologista unensäätelyä. Uni ei meinaa tulla tai se on pinnallista, koska keho on valmiina taistelemaan. Kun ei saa tai voi nukkua, elimistö joutuu koville ja immuunijärjestelmä alkaa pettää. Tämä voidaan havaita jo muutamien unettomien öiden jälkeen verenkuvassa lisääntyneellä tulehdusvasteella ja suoliston mikrobikannan heikentymisellä (Walker, 2018). Tiesitkö, että 80-90% serotoniini-välittäjäaineesta tuotetaan suolistossa? Jos suoliston bakteerikanta häiriintyy, esimerkkinä jatkuvasta unenpuutteesta, voiko se vaikuttaa haitallisesti serotoniinin tuotantoon? tuolla hyvän olon hormonilla on kuitenkin merkittävä rooli meidän tunteiden, vireystilan ja kivun käsittelyssä.
Unen aikana aivoissa tapahtuu ”huuhtelu”, jossa hermosolujen tuottamat jätteet huuhdotaan aivo-selkäydinnesteen mukana ”viemäriin”. Tätä järjestelmää kutsutaan glymfaattiseksi järjestelmäksi. Se huolehtii siitä, että keskushermostoon ei pääse kertymään haitallisia aineenvaihdunnan jäännöksiä, jotka ovat haitallisia hermosoluille. Päivän mittaan hermosolut tuottavat jätteitä, jotka voivat liiallisina määrinä tulehduttaa keskushermoston. Jos emme saa riittävästi syvää Nrem-unta, tämä hieno kehomme viemäriverkoston huuhtelu ei kykene aktivoitumaan. Tällöin hermosolujätteiden määrä kasaantuu ja kasaantuu ja kasaantuu, vuorokausi toisensa jälkeen. Tämä johtaa keskushermoston toiminnan häiriintymiselle ja heikkenemiselle. Se aktivoi immunologisen puolustusreaktion, joka tulehduttaa hermostoa.
Unenpuutteesta johtuva hermoston ylikuormittuminen vaikuttaa myös kipua sääteleviin järjestelmiin merkittävästi jo yhden huonosti nukutun yön jälkeen. Huonosti nukuttu yö laskee seuraavana päivänä kipukynnystä ja voimistaa entuudestaan päällä olevia kipuja. Fysiologiset kivun rektiot eivät toimi enää normaalisti ja aivot eivät kykene arvioimaan kipua oikein. Valvoneilla ihmisillä voidaankin todeta somatosensorisen eli aistitietoja käsittelevän aivokuoren voimakas aktivoituminen. (Krause et al. 2019)

Neuroinflammaatio voimistaa depressiota ja kipuja
Depressio eli masennustila voi ilmetä omana sairautenaan, mutta se on usein myös liitännäisoire esimerkiksi fibromyalgiassa, kroonisissa jännityspäänsäryissä ja CFS-syndroomassa (krooninen väsymysoireyhtymä). Depressioon liittyy usein myös kroonista särkyjä, unettomuutta, väsymystä, keskittymis- ja muistivaikeuksia. Polku on kuitenkin kaksisuuntainen; krooninen uniongelma voi kehittää depressio-oireiston. Depressio-oireiston mekanismeihin liittyy vahvasti keskushermoston mielialaa ja biologisia rytmejä säätelevien hermoverkostojen toiminnan häiriöt (Huttunen, 2018). Useammissa tutkimuksissa ja seurannoissa ollaan havaittu selvä korrelaatio jatkuvan pro-inflamatoristen sytokiinien korkean määrän ja masennusoireiden välillä ja se saattaa olla yhtenä masennuksen laukaisevana tekijänä (Zalli, 2016). Tutkimuksissa, jossa masentuneille annettiin pro-inflamatorisia sytokiineja, kokivat depresessio-oireiden pahenevan (Miller, 2009). Neuroinflamaation merkit masennuksessa on havaittu myös aivojen PET-kuvauksissa (Setiawan, et al. 2015).
Näistä voidaan todeta, että meidän terapeuttien tulisi selvittää pitkittyneistä kivuista kärsivän ihmisen stressin, depression ja unen määrää sekä unen laadullisia seikkoja. Tarvittaessa näihin tulisi puuttua valistamalla unen puutteen, stressin ja depression vaikutuksista kipuun ja tarvittaessa ohjata sopivalle terapeutille tai lääkärille. CBT-terapia (kognitiivinen behavioraalinen terapia) tai CBTI-terapia (kognitiivinen behavioraalinen terapia unettomuuteen) on tehokas menetelmä hoitaa stressiä ja unettomuutta (Morin et al. 1999; 2016). Oikeanlaisella stressin hallinnalla saadaan aikaan jopa aivokuvantamisessa havaittavia myönteisiä muutoksia (Porto, 2009) sekä verikokeissa havaittavia stressihormoni määrien laskua (Hannibal & Bishop, 2014).
Triggerpisteet osana neuroinflammatorista prosessia?
Myofaskiaaliset triggerpisteet ovat yksi tavallisimmista myofaskiaalisen kivun aiheuttajista, jossa spesifiä patologiaa ei pystytä todentamaan. Aktiiviset myofaskiaaliset kipupisteet esiintyvät usein jännityspäänsäryn, alaselkä-, niska-, leukanivel- ja yläraajakivun sekä lantion alueen kipuoireyhtymissä, mutta myös nivelrikossa, hermojuurioireissa, perifeerisissä hermopinteissä, reumasairauksissa ja fibromyalgiassa. Oireyhtymä voi aktivoitua myös mm. lihasvamman, lihasiskemian ja lihaksen toistuvan ylikuormituksen yhteydessä.
Myofaskiaalisen kivun patofysiologiaa ei edelleenkään tunneta täydellisesti. Vallitsevina hypoteeseina on kuitenkin myofaskiaalinen kudosiskemia, jonka metabolinen muutos ärsyttää liikehermopäätteitä aiheuttaen hermovälittäjäaine asetyylikoliinin vuotamisen synapsirakoon, jolloin postsynaptiset lihassyyt supistuvat (Gerwin et al. 2004). Näin hermolihasliitoksen ympärille muodostuu sähköisesti vaimea kontraktuura ja lihassyiden paksuunnos, joka omalta osaltaan heikentää kudoksen verenkiertoa ja hapensaantia, joka johtaa iskemiakierteeseen. Täytyy kuitenkin ymmärtää, että triggerpisteiden kehittyminen ei ole koskaan puhtaasti anatomisilla tai biomekaanisilla kuormitutekijöillä selittettävä ilmiö. Tähän liittyy vahvasti keskushermoston, autonomisen hermoston ja neuroimmunologian vaikuttavat tekijät perifeerisellä, selkäydin- ja supraspinaalisella tasolla.
Epäkäslihaksen kipupisteiden mikrodialyysissa on todettu aktiivisten triggerpisteiden ympärille kasaantuneen merkittävän paljon tulehdusaineita, kuten inflammatorisia sytokiineja (TNF-a, IL-1b, IL-6, IL-8) ja neuropeptidejä (supstanssi-P, CGRP, bradykiniini), verrattuna latentteihin triggerpisteisiin (Shah, J et al. 2008). Tämä selittää triggerpisteen kohonneen kipuherkkyyden (Verri et al. 2006). Kipupisteessä esiintyy myös hermolihasliitokseen liittyvää päätelevyaktiviisuutta ja spontaaneja päätelevypiikkejä merkittävästi useammin kuin kivuttomissa pisteissä.
Kyseessä on siis neuroimmunologisista syistä tulehtunut hermolihasliitos, joka aiheuttaa perifeerisen sensitisaation. Tämä muistuttaa hyvin paljon pienen pientä hermopinnettä, jossa jyllää neuroinflammaatio. Pitkään tulehtuneet triggerpisteet pommittavat jatkuvalla nosiseptiolla selkäytimen neuroneja, jotka voivat herkistyä ja alkaa läpäisemään herkemmin kipusignaaleja kohti aivoja (sentraalinen sensitisaatio). Triggerpisteillä on huomattavasti vahvempi vaikutus selkäytimen takasarven neuronien neuroplastisiin muutoksiin, kuin kudoksella, jossa ei ole triggerpistettä. Tämä johtuu suuremmasta määrästä triggerpisteisiin kytköksissä olevista pienistä sensorisista ja nosiseptiivisista neuroneista, joita on vähemmän kudoksessa, jossa ei ole triggerpistettä. (Kuan et al 2007)
Triggerpisteiden nosiseptio vahvistaa sentraalista sensitisaatiota ja neuroinfalmmaatiota
Esimerkiksi jatkuva triggerpisteiden hermopääteärsyke voi sensitisoida hermojuuren ganglion neuronit, johtaen hyperalgesiaan ja allodynaan, jossa spatiaalinen sekä temporaalinen summaatio on tärkeässä roolissa (Mense, 1994). Tämä selittää osittain sen, miksi triggerin säteily tai heijaste leviää useammalle tuntoalueelle. Tarkempi selitys tälle voi olla takajuuressa olevien uinuvien synapsien aktivoituminen. Lisätäkseni tähän vielä sen, että gliasolut, jotka ympäröivät afferentteja neuroneja, voivat voimistaa sentraalista sensitisaatiota takajuuren gangliossa. Erityisesti astrosyytit ja mikrogliat aktivoituvat välittäjäaine supstanssi-P:stä, ja näin ne saattavat alkaa tuottamaan inflammatorisia sytokiineja (TNF-a, IL-1 ja IL-6), jotka herkistävät kaikkien ganglioon kytkeytyvien hermojen neuronit (Watkins et al., 2007). Lisäksi takajuuren ganglion ärsytys vapauttaa lisää supstanssi-P:tä hermon distaalipäässä, joka ylläpitää tulehduskierrettä (Buttler, 2000).
Kivuttomilla ihmisillä latenttien triggerpisteiden mekaanisella stimulaatiolla voidaan saada aikaan väliaikainen sentraalinen sensitisaatio, joka voidaan havaita mekaanisenaa hyperalgesiana pisteen ulkopuolisella hermotusalueella (extrasegmentaalinen alue), kuten täysin toisessa lihaksessa tai jopa vastakkaisessa raajassa. (XU et al 2010). Esimerkiksi EMG-mittauksissa infraspinatuksen triggerpisteen kohonnut hermopääteaktiviteetti nostaa saman raajan extensor carpi radialis previs -lihaksen hermopääteaktiviteettia (Fernándes-Carnero et al 2010). Voidaan siis olettaa, että aktiiviset triggerpisteet voivat aiheuttaa keskushermoston herkistymistä, mutta polku on kaksi suuntainen – keskushermoston herkistyminen saa aikaan triggerpisteiden aktiviteetin kohoamisen. Triggerpisteiden herkistyminen on osittain myös supraspinaalisella tasolla olevien mekanismien aikaan saannosta. Hippokampuksen epänormaalin hypoaktiviteetin ja sympaattisen hermoston ”taistele tai pakene” refleksin aktivoituminen on havaittu voimistavan triggerpisteiden aktiopotentiaalista jännitettä ja kehittävän pisteisiin liittyvää hyperalgesiaa (Niddam et al 2008; 2009).
Lähteet
Abdallah C. 2017. Chronic Pain and Chronic Stress: Two Sides of the Same Coin? https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5546756/
Butler D. 2000. The sensitive nervous system. Noigroup Puplications.
Dommerholt J. 2006. Myofascial trigger points: An evidence-informed review https://www.researchgate.net/publication/289505749_Myofascial_trigger_points_an_evidence-informed_review
Fernandez-Carnero. 2010. Increased spontaneous electrical activity at a latent myofascial trigger point after nociceptive stimulation of another latent trigger point. https://www.ncbi.nlm.nih.gov/pubmed/20090441
Gerwin RD. 2004. An expansion of Simons’ integrated hypothesis of trigger point formation. https://www.ncbi.nlm.nih.gov/pubmed/15509461
Hannibal Ke. Bishop MD. 2014. Chronic stress, cortisol dysfunction, and pain: a psychoneuroendocrine rationale for stress management in pain rehabilitation. https://www.ncbi.nlm.nih.gov/pubmed/25035267
Kuan et al. 2007. The spinal cord connections of the myofascial trigger spots.https://www.ncbi.nlm.nih.gov/pubmed/17174128
Krause et al. 2019. The pain of sleep loss: a brain characterization in humans http://www.jneurosci.org/content/39/12/2291
Mense 1994. Referral of muscle pain. https://www.jpain.org/article/S1058-9139(05)80227-X/abstract
Miller A, at al. 2009. Inflammation and Its Discontents: The Role of Cytokines in the Pathophysiology of Major Depression. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2680424/
Morin et al. 1999. Nonpharmacologic treatment of chronic insomnia. An American Academy of Sleep Medicine review. https://www.ncbi.nlm.nih.gov/pubmed/10617176
Morin et al 2006. Psychological and behavioral treatment of insomnia:update of the recent evidence (1998-2004). https://www.ncbi.nlm.nih.gov/pubmed/17162986
Niddam et al 2008. Central representation of hyperalgesia from myofascial trigger point. https://www.sciencedirect.com/science/article/pii/S1053811907008865
Niddam et al 2009. Brain manifestation and modulation of pain from myofascial trigger points. https://www.ncbi.nlm.nih.gov/pubmed/19728963
Page, 2004. Arethere long-term consequences of pain in newborn or very young infants? https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1595204/
Porto PR. 2009. Does cognitive behavioral therapy change the brain? A systematic review of neuroimaging in anxiety disorders. https://www.ncbi.nlm.nih.gov/pubmed/19622682
Quintner JL. 2015. A critical evaluation of the trigger point phenomenon.https://academic.oup.com/rheumatology/article/54/3/392/1796114
Ren & Dubner, 2010. Interactions between the immune and nervous systems in pain https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3077564/
Salter, 2018. RELIEF: Pain research news. Alexander Tuttle. https://relief.news/pain-101-how-the-immune-system-influences-chronic-pain/
SAPOLSKY, R. 1998. Why zebras don’t get ulcers. An updated guide to stress, stressrelated diseases and coping, Freemanhttps://www.mta.ca/pshl/docs/zebras.pdf
Setiawan E, et al. 2015. Role of translocator protein density, a marker of neuroinflammation, in the brain during major depressive episodes. https://www.ncbi.nlm.nih.gov/pubmed/25629589
Shah J et al. 2008. Uncovering the biochemical milieu of myofascial trigger points using in vivo microdialysis: An application of muscle pain concepts to myofascial pain syndrome http://drsvanderveen.info/PDF/Shah_Biological_milieu_of_MTP.pdf#page14
Shah J. 2015. Myofascial Trigger Points Then and Now: A Historical and Scientific Perspective https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4508225/
Totsch & Sorge, 2017. Immune system involvement in specific pain conditions. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5555497/
Verri, W.A. Et al, 2006. Hypernociceptive role of cytokines and chemokines: targets for analgesic drug development? https://www.ncbi.nlm.nih.gov/pubmed/16730375
Walker, M. 2018. Why we sleep? The new science of sleep and dreams. Penguin Books ltd.
Xiaoqiang Z. et al. 2014. Understanding of myofascial trigger points https://www.researchgate.net/publication/269999790_Understanding_of_myofascial_trigger_points
Xu. Et al. 2010. Sustained nociceptive mechanical stimulation of latent myofascial trigger point induces central sensitization in healthy subjects. https://www.ncbi.nlm.nih.gov/pubmed/20451466
Zalli A. 2016. Low-grade inflammation predicts persistence of depressive symptoms https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4828485/